Реакции, протекающие с изменением степени окисления атомов, входящих в состав реагирующих веществ, называются окислительно-восстановительными.
Изменение степени окисления связано с оттягиванием или перемещением электронов.
Рассмотрим основные положения теории окислительно-восстановительных реакций.
1. Окислением называется процесс отдачи электронов атомом, молекулой или ионом.
При окислении степень окисления повышается.
2. Восстановлением называется процесс присоединения электронов атомом, молекулой или ионом.
При восстановлении степень окисления понижается.
3. Атомы, молекулы или ионы, отдающие электроны называются восстановителями. Во время реакции они окисляются. Ато¬мы, молекулы или ионы, присоединяющие электроны, называются окислителями. Во время реакции они восстанавливаются. Так как атомы, молекулы и ионы входят в состав определенных ве¬ществ, то и эти вещества соответственно называются восстановителями или окислителями.
4. Окисление всегда сопровождается восстановлением, и наоборот, восстановление всегда связано с окислением, что можно выразить уравнениями:
Восстановитель – е- = Окислитель
Окислитель + е- = Восстановитель
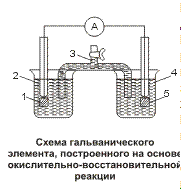
Процессы окисления и восстановления можно физически отделить друг от друга и осуществить перенос электронов по внешней электрической цепи. Пусть в стакан 2 налит раствор иодида калия КI , а в стакан 4 - раствор хлорида железа (III) FeСl3. Растворы соединены между собой так называемым «электролитическим ключом» 3 – U-образной трубкой, заполненной раствором хлорида калия КCl, обеспечивающим ионную проводимость. В растворы опущены платиновые электроды 1 и 5. Если замкнуть цепь, включив в нее чувствительный амперметр, то по отклонению стрелки можно будет наблюдать прохождение электрического тока и его направление.
Всякая окислительно-восстановительная реакция может служить источником электрического тока, если она протекает в гальваническом элементе
Совокупность ОВР , которые протекают на электродах в растворах или расплавах электролитов при пропускании через них электрического тока, называют электролизом.
На катоде источника тока происходит процесс передачи электронов катионам из раствора или расплава, поэтому катод является «восстановителем». На аноде происходит отдача электронов анионами, поэтому анод является «окислителем».
Изменение степени окисления связано с оттягиванием или перемещением электронов.
Рассмотрим основные положения теории окислительно-восстановительных реакций.
1. Окислением называется процесс отдачи электронов атомом, молекулой или ионом.
При окислении степень окисления повышается.
2. Восстановлением называется процесс присоединения электронов атомом, молекулой или ионом.
При восстановлении степень окисления понижается.
3. Атомы, молекулы или ионы, отдающие электроны называются восстановителями. Во время реакции они окисляются. Ато¬мы, молекулы или ионы, присоединяющие электроны, называются окислителями. Во время реакции они восстанавливаются. Так как атомы, молекулы и ионы входят в состав определенных ве¬ществ, то и эти вещества соответственно называются восстановителями или окислителями.
4. Окисление всегда сопровождается восстановлением, и наоборот, восстановление всегда связано с окислением, что можно выразить уравнениями:
Восстановитель – е- = Окислитель
Окислитель + е- = Восстановитель
Процессы окисления и восстановления можно физически отделить друг от друга и осуществить перенос электронов по внешней электрической цепи. Пусть в стакан 2 налит раствор иодида калия КI , а в стакан 4 - раствор хлорида железа (III) FeСl3. Растворы соединены между собой так называемым «электролитическим ключом» 3 – U-образной трубкой, заполненной раствором хлорида калия КCl, обеспечивающим ионную проводимость. В растворы опущены платиновые электроды 1 и 5. Если замкнуть цепь, включив в нее чувствительный амперметр, то по отклонению стрелки можно будет наблюдать прохождение электрического тока и его направление.
Всякая окислительно-восстановительная реакция может служить источником электрического тока, если она протекает в гальваническом элементе
Совокупность ОВР , которые протекают на электродах в растворах или расплавах электролитов при пропускании через них электрического тока, называют электролизом.
На катоде источника тока происходит процесс передачи электронов катионам из раствора или расплава, поэтому катод является «восстановителем». На аноде происходит отдача электронов анионами, поэтому анод является «окислителем».