|
Назад
|
Всероссийская олимпиада школьников по химии 2005/2006 гОбластной этап. Экспериментальный тур. Получение газов в лаборатории Задание 1. Из приборов, используемых для получения газов наиболее удобны автоматические приборы, в которых реакция прекращается, как только газоотводную трубку закрывают зажимом. В вашем распоряжении пробирка с отверстием в донышке, пробка, трубки, зажим, другое оборудование. Предложите конструкцию автоматического прибора, с помощью которого можно получать такие газы, как водород, оксид углерода(IV) и собирать эти газы методом вытеснения воды. Зарисуйте прибор, укажите, где будут размещаться исходные вещества, полученный газ, объясните принцип действия прибора, напишите соответствующие уравнения реакций. Как можно доказать наличие этих газов в пробирках? Напишите уравнения реакций, укажите признаки их протекания.
"- - - - - - - - - -- - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - -
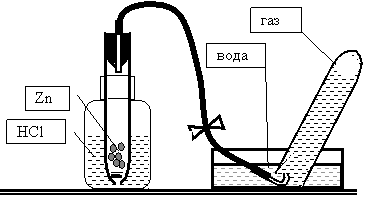
Задание 2. (Выдается отдельно, после выполнения задания 1) Соберите прибор согласно рисунку и образцу. На дно пробирки с отверстием положите 1-2 пластмассовых кружка, склянку прибора закрепите в лапке штатива.
Отвесьте около 3-х граммов цинка (точную массу запишите), загрузите в прибор, закройте зажим газоотводной трубки. Залейте в склянку прибора 50 мл кислоты, отмерив ее объем цилиндром. Опустите пробирку в кислоту. Протекает ли реакция? Опробуйте работу прибора, открывая и закрывая зажим газоотводной трубки. Соберите газ в пробирку методом вытеснения воды. Когда пробирка заполнится полностью, закройте ее пробкой, и сдайте преподавателю. Аккуратно выньте пробирку прибора, отсоедините газоотводную трубку, промойте цинк водой и перенесите его на лист фильтровальной бумаги. Отвесьте около 3-х граммов мрамора (точную массу запишите), загрузите в прибор и повторите опыт, собрав полученный углекислый газ во вторую пробирку. Сдайте пробирку с газом преподавателю, оставшийся мрамор также промойте и выложите на лист фильтровальной бумаги. Взвесьте оставшиеся после опыта высушенные вещества (цинк и мрамор). Рассчитайте выход газа (в процентах от теоретического) для первой и второй реакции. Объясните полученные результаты.
"- - - - - - - - - -- - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - -
Решения экспериментального тура. Задание 1. а) Конструкция прибора ясна из задания 2, принцип действия основан на том, что при закрывании газоотводной трубки, выделяющийся газ вытесняет кислоту из пробирки и реакция прекращается. Уравнения реакций: Zn +2HCl = ZnCl2 + H2; CaCO3 + 2HCl = CaCl2 + H2O + CO2 Доказать наличие водорода проще всего по его горючести: 2H2 + O2 = 2H2O Если водород в пробирке чистый – он сгорает со слабым
звуком. Если водород содержит примесь воздуха – звук резкий, свистящий.
Задание 2. Пример расчетов: Пусть масса цинка до реакции 3 г, после реакции 2,8 г. Значит в реакцию вступило 0,2 г цинка, n(Zn) = n(H2) = m/M = 2/65=0,00308 моль, Vтеор(H2) = nVM = 0,00308*22,4 = 0,069 л = 69 мл. Если объем пробирки составлял 50 мл: выход: h =Vпр/ Vтеор = 50/69 = 0,725 = 72,5% Оценивание: Задание 1. Конструкция прибора и принцип действия по 2 балла, уравнения реакций 1 балл, всего 5 баллов Задание 2. Техника работы 5 баллов, отчет, ответы на вопросы и расчет выхода 5 баллов, качество продукта 2 балла. Дополнительные баллы участникам, первыми закончившим эксперимент, за быстроту и аккуратность в работе, при условии правильного выполнения и достаточно полного описания хода работы – до 3 баллов Суммарная оценка 20 баллов.
Можаев Г. М., старший преподаватель |
||||
| . | |||||
 Определите и запишите объем пробирок, выданных для
собирания газов.
Определите и запишите объем пробирок, выданных для
собирания газов.