Районная олимпиада школьников по
химии 2007/2008 г.
Девятый класс.
Задача 9-1.
Предельно допустимая концентрация (ПДК) оксида углерода(II) в атмосферном воздухе равна 3 мг/м3. Вычислите объёмную долю СО в атмосферном воздухе при предельно допустимой концентрации СО и число молекул оксида углерода(II) в 1 м3 воздуха (н.у.). Какое тривиальное название вы знаете для этого вещества? Как оно образуется и чем опасно?
(6 баллов)
Задача
9-2.
В 106,5 г 6%-ного раствора сульфата натрия дополнительно растворили 9,99 г кристаллогидрата Al2(SO4)3*18H2O. Определите, каких ионов, натрия или сульфат-ионов, катионов или анионов, будет больше в полученном растворе. Какими способами можно доказать наличие каждого из ионов в этом растворе? Напишите соответствующие ионные уравнения реакций
(7 баллов)
Задача
9-3.
Для реакции с оксидом азота(V) использовали 200 г известкового молока с содержанием гидроксида кальция 1,85%. Какие вещества могли образоваться при этом? Напишите уравнения реакций. Рассчитайте массу образовавшейся соли, если известно, что в реакции участвовало 6,48 г оксида азота(V).
(7 баллов)
Задача
9-4.
Смесь кислорода с водородом объемом 3 л воспламенили, остаток охладили до комнатной температуры, причем объем газа составил 1,8 л. Каков мог быть состав исходной газовой смеси (в объемных долях)? Как можно установить его однозначно?
(6 баллов)
Задача 9-5.
Разновидность атомов одного из химических элементов содержит в своем составе 114 элементарных частиц, причем число нейтральных частиц на 9 больше числа отрицательных. Что это за частицы? Охарактеризуйте строение ядра и электронной оболочки атома, а также основные химические свойства данного элемента.
(8 баллов)
Районная олимпиада школьников по
химии 2007/2008 г.
Деcятый класс.
Задача 10-1.
Для полного сгорания 0,1 моль алкана потребовалось 14,56 л кислорода (н.у.). Установите формулу алкана. Существуют ли изомеры у этого вещества? Если да, напишите их структурные формулы и дайте названия по международной номенклатуре.
(5 баллов)
Задача 10-2.
При охлаждении 150 г раствора нитрата бария насыщенного при 80°С часть соли выпала в осадок, а массовая доля нитрата бария в растворе уменьшилась с 21% до 8,34%. Выпавшие кристаллы растворили в воде и довели объем этого раствора до 1 л. Чему будет равна молярная концентрация полученного раствора? Какое примерно число анионов будет содержаться в 1 мл этого раствора? (9 баллов)
Задача 10-3.
При взаимодействии цинка с разбавленой азотной кислотой образуется оксид азота(I) с выходом 35%. Рассчитайте массу цинка и 20%-ной азотной кислоты, необходимых для получения 1,12 л этого газа (н.у.).
(7 баллов)
Задача 10-4.
После растворения смеси нитрата серебра и бромида калия в воде образовался осадок, масса которого оказалась в 1,2 раза больше массы солей в полученном растворе. Определите состав исходной смеси, если известно, что в полученном растворе отсутствуют ионы серебра.
(9 баллов)
Задача 10-5.
Определите элементы, зашифрованые буквами Х и Y, если известно, что на внешнем слое электронной оболочки Х находится 5 электронов, а раствор YCl2 бледно-зеленого цвета. Напишите уравнения реакций, укажите условия их протекания:
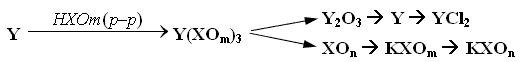
(7 баллов)
Районная олимпиада школьников по
химии 2007/2008 г.
Одиннадцатый класс.
Задача 11-1.
В реакции этерификации израсходовалось 11,1 г одноатомного первичного спирта, 9 г карбоновой кислоты и было получено 17,4 г сложного эфира. Определите формулу эфира и назовите его. Предложите формулы как минимум еще двух веществ, являющихся изомерами этого эфира, но относящихся к другим классам веществ.
(9 баллов)
Задача 11-2.
В толстостенном сосуде взорвали смесь 12 мл метана и 130 мл воздуха. За счет выделившейся теплоты сосуд разогрелся до температуры 150°С. Рассчитайте состав полученной газовой смеси в объемных долях при этой температуре. Как изменится ее состав после охлаждения сосуда до 0°С? (Считать, что в воздухе 21% по объему кислорода и азот, содержанием других веществ пренебречь)
(5 баллов)
Задача 11-3.
Для нейтрализации 50г 15%-ной соляной кислоты к ней добавили 55 г 5,6%-ного раствора гидроксида калия, а потом некоторый объем 12,5%-ного раствора карбоната натрия. Определите состав (массовые доли) полученного при нейтрализации раствора.
(8 баллов)
Задача 11-4.
Как распознать без помощи дополнительных реактивов водные растворы следующих веществ: хлорид меди(II), хлорид цинка, соляную кислоту, едкий натр, соду, хлорид кальция. Составьте план анализа и напишите соответствующие уравнения реакций.
(6 баллов)
Задача 11-5.
Аммиак, полученный при взаимодействии с водой 12 г нитрида магния, поглотили 120 мл раствора ортофосфорной кислоты с концентрацией 1,25 моль/л. Назовите вещества, которые будут содержаться в полученном растворе, рассчитайте их массы.
(8 баллов)
|